Una reacción química es un proceso en el que una sustancia o más sustancias cambian para formar uno o más sustancias nuevas. Con el objetivo de escribir una reacción, los químicos han desarrollado una forma estándar para representarlas por medio de ecuaciones químicas. Una ecuación química utiliza símbolos químicos para demostrar que sucede durante una reacción química.
CRACTERISTICAS
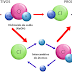
-En una reacción química los átomos no cambian, lo que cambia son los enlaces que los unen.
-La mayoría de las reacciones ocurren en soluciones acuosas.
-Pueden ser reversibles, si los productos pasan a ser reactantes o irreversibles, cuando los productos no vuelven a formar los reactivos que le dieron origen.
-Las reacciones pueden ser simples, cuando requieren un solo paso para que los reactivos se conviertan en productos o complejos, cuando pueden presentar varios pasos entre los reactivos y el productos, pudiendo formar además, compuestos intermedios.
- Los átomos se mantiene, la cantidad de átomos en los reactantes es igual a la cantidad de átomos en los productos.
Hay varios tipos de reacciones químicas. Algunos de los más comunes son:
1. Reacción de síntesis (o combinación): Dos o más sustancias se combinan para formar un solo producto. Ejemplo: A + B → AB
2. Reacción de descomposición: Una sustancia se descompone en dos o más productos.
Ejemplo: AB → A + B
3. Reacción de sustitución simple: Un elemento reemplaza a otro en un compuesto.
Ejemplo: A + BC → AC + B
4. Reacción de doble sustitución (o metátesis): Los componentes de dos compuestos intercambian lugares. Ejemplo: AB + CD → AD + CB
5. Reacción de oxidación-reducción (redox): Implica transferencia de electrones entre sustancias. Oxidación es la pérdida de electrones y reducción es la ganancia. Ejemplo: A + B → A+ + B-
6. Reacción de combustión: Una sustancia reacciona con el oxígeno y produce calor, luz y generalmente dióxido de carbono y agua. Ejemplo: CH4 + 2O2 → CO2 + 2H2O
7. Reacción ácido-base: Un ácido y una base reaccionan para formar agua y una sal. Ejemplo: HCl + NaOH → H2O + NaCl
8. Reacción de precipitación: Dos soluciones acuosas reaccionan para formar un precipitado insoluble. Ejemplo: AgNO3 + NaCl → AgCl↓ + NaNO3
EJEMPLO DE REACCION QUÍMICA
Reacción del vinagre y la cáscara de huevo
El vinagre es una solución de ácido acético CH3COOH, que es un ácido orgánico débil. La cáscara del huevo está formada por carbonato de calcio CaCO3. Cuando colocamos un huevo en vinagre, podemos observar la aparición de unas burbujas (el dióxido de carbono) y al cabo de un tiempo la cáscara pierde su rigidez.
La reacción que se produce entre el carbonato de calcio y el ácido acético produce acetato de calcio CH3COOCa y dióxido de carbono CO2:



No hay comentarios.:
Publicar un comentario